Endokrinologi
-

Fråga efter symtom på hypogonadism hos män med depressiva besvär
Den generella uppfattningen bland läkarna är att män med hypogonadism är svåra att diagnostisera. En av förklaringarna kan vara att de diagnostiska kriterierna för testosteronbrist är ganska diffusa.
-

Så bör du som läkare resonera vid frågor om testosteronbrist
Vad räknas som testosteronbrist och vilka ska behandlas? Här pågår det ett intensivt kunskapssökande runt om i världen just nu, menar Mats Holmberg, androlog och endokrinolog vid Karolinska Universitetssjukhuset.
-

Så är det att leva med hypogonadism
Manlig hypogonadism ger ofta diffusa symtom och det kan vara svårt att ställa diagnos. I en patientenkät berättar män om hur de upplever sin testosteronbrist, vilket kan vara till hjälp för att känna igen dessa patienter.
-

Testosteronbrist: 6 utmaningar för dig som primärvårdsläkare
Det finns flera utmaningar vid utredning och behandling av testosteronbrist. Mikael Lehtihet, docent och överläkare i endokrinologi vid Capio S:t Görans sjukhus, går igenom några av dem.
-
Forskare: Utvecklingen inom sköldkörtelvården har stannat av
Netdoktor frågar politiker, läkare och patientföreträdare om vad de vill se för åtgärder inom sköldkörtelvården.
-
En av fyra sköldkörtelsjuka blir inte hjälpta av standardbehandlingen
De flesta patienter med hypotyreos mår bra av standardbehandling baserad på substansen levotyroxin (T4). "Då majoriteten blir bra anser man att behandlingen funkar. Men vi måste kunna behandla de andra patienterna också och då fungerar inte standardbehandlingen", säger Kerstin Brisma, specialist i endokrinologi.
-
Tips om akut endokrinologi
Överläkare Mats Palmér ger värdefulla tips när han föreläser om akut endokrinologi på AT-stämman.
-
Att kvalitetssäkra framtidens vård
Vårdpersonal stöter dagligen på problem på sin arbetsplats som påverkar både arbetsmiljön och patientsäkerheten. Vi i "Arbetsgruppen för vårdreform" menar att den bristande kommunikationen mellan de anställda och beslutsfattarna måste åtgärdas.
-

Manlig hypogonadism
Testosteronbrist, så kallat hypogonadism, ger ofta diffusa symtom och det kan vara svårt att ställa diagnosen enbart utifrån kliniska förhållanden. Man skiljer mellan primär, sekundär och övrig hypogonadism.
-

Diabetes mellitus typ 1
Blodglukosstegring på grund av bristande egenproduktion av insulin. Någon helt entydig klar definition för avgränsning av tillståndet mot andra diabetestyper finns inte men låg c-peptid och förekomst av ö-cellsantikroppar stärker diagnosen.
-
Hyperaldosteronism, primär
Hyperaldesteronism innefattar olika tillstånd med förhöjda aldesteronnivåer i blodet. Denna text handlar främst om primär hyperaldosteronism, PA, som är den vanligaste orsaken till sekundär hypertoni.
-
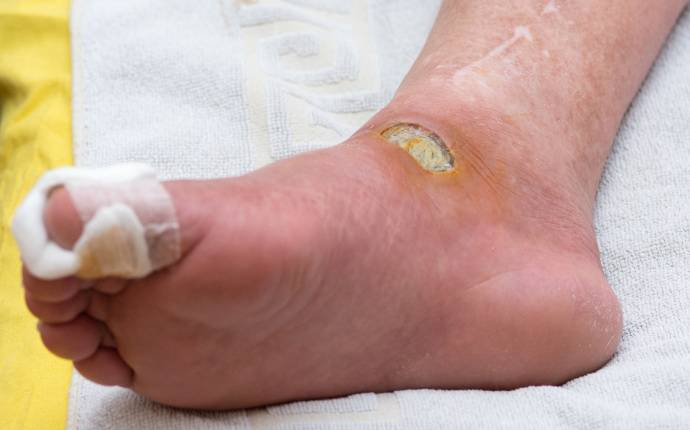
Diabetesfotsår (diabetesfot)
Cirka 25 procent av alla med diabetes får ett diabetesfotsår, som uppstår som en följd av senkomplikationerna neuropati och perifer arteriell sjukdom. Utredningen bygger på anamnes och kliniska fynd.
-
D-vitaminbrist