Livmoderhalscancer (cervixcancer)
De två dominerande cancersjukdomarna som uppstår i livmodern är livmodershalscancer (cervixcancer) och livmoderkroppscancer (corpuscancer). Globalt är cervixcancer en av de vanligaste cancerformerna hos kvinnor.
Definition av livmoderhalscancer
Vad vet du om biosimilarer?
Vi på NetdoktorPro vore tacksamma om du ville genomföra enkäten som bara tar några minuter. Du får samtidigt uppdaterade kunskaper om t ex vad som krävs för att en biosimilar ska godkännas, skillnaden mellan ett generiskt läkemedel och biosimilarer och vad som egentligen menas med en "switch".
Kongressbevakning
NetdoktorPro rapporterar från ESMO
Följ vår kongressbevakning från ESMO (European Society of Medical Oncology) och ta del av bland annat kongressrapporter, referat och intervjuer med kollegor som deltagit.
Indelning
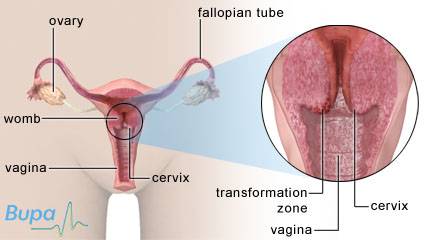
Livmoderhalsen är den nedre delen av livmodern. Den går ner i slidan och avslutas med livmodertappen, även kallad ”portio” (egentligen portio vaginalis uteri). Livmoderhalsen och livmodertappen är täckta av skivepitel respektive körtelepitel som möts i ett område på livmodertappen. Gränsen mellan celltyperna kallas för transformationszon eller ”squamo-columnar junction” och är predilektionsstället för cancerutveckling.
Olika varianter av livmoderhalscancer (cancer i cervix)
Av all cervixcancer som diagnostiseras är cirka 85 procent skivepitelcancer - majoriteten av övriga fall utgörs av adenocarcinom. Även till exempel sarkom förekommer, men är sällsynt. Adenocarcinomen tenderar att öka både i relativa och absoluta tal, medan skivepitelcancer har minskat drastiskt sedan man införde screening. Genom kolposkopi, histopatologi och cellprovtagning kan man bedöma portios epitel och diagnostisera olika varianter av dysplasier (cellförändringar).
Dysplasierna brukar indelas i tre grader (lätta, måttliga, svåra), enligt Richart benämnt som Cervical Intraepithelial Neoplasia (CIN) I-III. Även termen CIS (cancer in situ) används och är liktydig med CIN III, det vill säga svår, eller stark, dysplasi. Cirka 10-20 procent av dysplasierna utvecklas till invasiv cancer, medan övriga blir stationära eller regredierar. Sedan 1988 används även ett klassificeringssystem, ”the Bethesda system”, reviderat 1991. I systemet används begreppet Squamous Intrepithelial Lesion (SIL). Low Grade SIL inkluderar CIN 1 och koilocytotiska skador, High Grade SIL inkluderar CIN II och III.
Vill du bli först med att ta del av NetdoktorPro:s nyhetsrapportering från kongressen ESMO (European Society of Medical Oncology)? Lämna din e-postadress här »
Vad vet du om biosimilarer?
Vi på NetdoktorPro vore tacksamma om du ville genomföra enkäten som bara tar några minuter. Du får samtidigt uppdaterade kunskaper om t ex vad som krävs för att en biosimilar ska godkännas, skillnaden mellan ett generiskt läkemedel och biosimilarer och vad som egentligen menas med en "switch".
Bakgrund och epidemiologi
Epidemiologiska data stöder sedan decennier hypotesen att HPV (humant papillomvirus) har en etiologisk betydelse för uppkomsten av livmoderhalscancer, cervixcancer, och HPV är allmänt accepterad som primär kausal orsak till cervixcancer och dess förstadier.
HPV förekommer i cirka 80 procent vid CIN/SIL (mätt med polymerase chain reaction, PCR). Främst är det de hög-onkogena HPV-typerna 16, 18 och 31 som ger höggradig CIN/SIL och invasiv cancer. Även andra typer förekommer, som HPV 6, 11, 42, 43, 44, 45, 51, 52, 56 och 58 (låg-onkogena). Intermediär-onkogena typer är 33, 35, 39, 51 och 52. I över 20 procent av fallen förekommer fler än en typ av HPV.
Kondom skyddar inte mot HPV-infektion. Tvärtom korrelerar kondom- och pessaranvändande med cervixcancer, dock endast svagt. Alla med virusinfektion utvecklar inte livmoderhalscancer och det finns även HPV-negativa cancerfall, vilket talar för att HPV-infektion ensam inte är en tillräcklig etiologisk förklaring.
Incidensen av cervixcancer
Livmoderhalscancer är ovanligt före 25 års ålder. Vanligast är sjukdomen mellan 30 och 40 samt efter 70 års ålder. Det kan bero på att äldre kvinnor inte regelbundet har genomgått cellprov, eller bero på någon okänd etiologisk faktor, vars carcinogena effekt är dröjande. Sedan 1960-talet erbjuds alla svenska kvinnor mellan 23 och 60 år regelbunden gynekologisk cellprovstagning. Före införandet av screeningen i Sverige låg incidensen (antal nya fall under ett år) av cervixcancer på cirka 900 fall årligen. Därefter har cervixcancer fallit från tredje till sjuttonde plats i statistiken över nya cancerfall hos svenska kvinnor. Tendensen är densamma i andra länder som infört screeningprogram.
Incidensen i Sverige har alltså sjunkit sedan 1960-talet, och i den senaste statistiken från 2011 noterades 421 nya fall det året. Statistiken över prevalensen (antal individer med sjukdomen vid en viss tidpunkt) är något osäkrare och redovisas inte längre samlat som tidigare, men enligt rapporteringen var prevalenstalet cirka 10 000 år 2000 i Sverige. Den relativt höga prevalensen i förhållande till incidensen speglar att sjukdomen drabbar många relativt unga individer samt att överlevnaden är god. Mortaliteten (antalet döda eller andelen dödsfall i en population) var år 2012 180 svenska kvinnor. Efter det att screening införts i Sverige sjönk mortaliteten initialt med 60 procent, men därefter har femårsöverlevnaden legat tämligen konstant kring 70 procent.
Globalt inträffar årligen cirka 470 000 nya fall av cervixcancer, vilket utgör ungefär 10 procent av all cancer hos kvinnor. Mer än hälften av de drabbade dör i sin sjukdom. 80 procent av fallen drabbar kvinnor i utvecklingsländerna, där sjukdomen ibland benämns som ”the great killer”.
TIPS: Vill du bli först med att ta del av NetdoktorPro:s nyhetsrapportering från kongressen ESMO (European Society for Medical Oncology)? Lämna din e-postadress här »
Etiologi och patogenes
Angående HPV som etiologisk faktor, var god se ovan. Ytterligare etiologiska faktorer, med eller utan koppling till HPV, finns. HPV-infektion och dysplasier är överrepresenterade hos patienter med kraftigt nedsatt immunförsvar, till exempel transplanerade patienter och patienter med AIDS. P-piller har ett direkt samband med cervixcancer, och indirekt med HPV-infektion, och studier ger stöd för att p-piller kan potentiera HPV-aktivitet.
Rökning förekommer i ökad frekvens hos patienter med cervixcancer, men tycks inte korrelera till utveckling av dysplasigrad. Detta trots att tobaksmetaboliter förekommer i 50 gånger högre koncentration i cervixsekret jämfört med i plasma. Rökning korrelerar dock starkt med HPV-infektion, vilket talar för något slags indirekt samband med cervixcancer. Om man korrigerar för HPV-infektion, kvarstår en viss korrelation med antal partners, ålder vid första samlag och antal samlag före 20-års ålder. Det inger misstanke om att samtidig förekomst av andra genitala infektioner kan ha betydelse.
Livmoderhalsen och livmodertappen är täckta av skivepitel respektive körtelepitel, vilka möts i ett område på livmodertappen. Slemhinnan är där extra känslig för angrepp av bakterier och virus, som kan skada cellerna. Cellförändringar kan då uppstå, och dessa kan så småningom kan utvecklas till cancer.
Klinisk bild
Förstadier till livmoderhalscancer ger inga symtom, utan kan bara upptäckas vid aktiv testning, som idag görs vid en gynekologisk cellprovtagning. Även om man har fullt utvecklad livmoderhalscancer i tidigt stadium kan man vara utan symtom.
Det vanligaste symtomet på livmoderhalscancer är blödningar från underlivet. De kan till en början komma efter samlag eller i samband med ansträngningar som till exempel vid toalettbesök. Efter ett tag uppstår blödningarna oftare, och till slut mer eller mindre dagligen. Om cancern har spridit sig utanför livmodern kan man få ont på ett sätt som påminner om mensvärk. Även benen kan svullna, vilket då beror på stas i vener eller lymfsystemet på grund av loko-regional spridning eller överväxt.
Det klassiska symtomet vid cervixcancer (som får kvinnan att söka läkare) är kontaktblödningar, det vill säga blödningar som uppstår vid samlag. Blödningarna är sällan förenade med smärta. Det kan även vara andra former av olaga blödningar från vagina, till exempel vid ansträngning eller vid defekation. Vanligt är också flytningar, oftast illaluktande och som inte upphör trots antibiotikabehandling. Tumorös och nekrotisk vävnad är predilektionsställen för bakteriella infektioner som kan leda till vaginiter och cerviciter med flytningar - men också till salpingiter och infektioner i parametriet, med uttalade smärtor och feber som följd. Flytningar, blödningar och smärtor i nedre delen av buken skall alltid följas upp med gynekologisk undersökning och eventuell provtagning. Allmänna symtom som viktnedgång, aptitlöshet, tarmstörningar och blåspåverkan är symtom förenade med avancerat tumörstatus.
NetdoktorPro rapporterar från ESMO
Följ vår kongressbevakning från ESMO (European Society of Medical Oncology) och ta del av bland annat kongressrapporter, referat och intervjuer med kollegor som deltagit.
Diagnos och undersökning
Svenska kvinnor mellan 23 och 49 år erbjuds cellprovtagning var tredje år, och mellan 50 och 60 år var femte år. Kvinnor som genomgått behandling för höggradig dysplasi bör följas med cellprov minst 25 år efter behandling (Strander, 2011). Årligen tas cirka 600 000 ”cellprov” i screening-programmet. Ytterligare cirka 100 000 cellprov tas vid sidan av programmet eller utgörs av provtagning som del i vidare utredning eller uppföljning efter åtgärd. Varje år har cirka 20 000 kvinnor ett screeningprov som är avvikande och kräver någon typ av utredning.
Undersökningen kan göras av läkare eller utbildad barnmorska och består av en gynekologisk undersökning och cellprovstagning från vagina (bakre fornix), portio och cervixkanalen. Cellproven kallas för ”Pap smear” efter Papanicolau som utvecklade metoden som lanserades 1943. Det görs närmare en miljon Pap smears årligen i Sverige. Upp mot en fjärdedel av proven visar CIN I-III och cirka 0,05 procent är maligna eller misstänkt maligna.
De patienter som fångas vid screening har som regel inga eller mycket diskreta symtom. Ibland kan man dock redan vid denna tidpunkt se tumörsuspekta förändringar på portio i form av sår eller exofytisk, tumorös vävnad. Vid palpation kan man ibland också känna en tunnformad cervix som är typisk för endocervikal växt. Liknande fynd kan göras vid en gynekologisk undersökning och skall då alltid följas upp med adekvat provtagning, provexcision eller skrap.
Utredning
Om man har symtom, eller om ett cellprov har visat cellförändringar, behöver man genomgå en gynekologisk undersökning, vanligtvis på en gynekologisk mottagning. Vid undersökningen används kolposkop för att bättre se eventuella förändringar på livmodertappen. Det tas också vävnadsprov. I samband med undersökningen kommer patienten och läkare överens om när svar på proverna ska lämnas.
När misstanke föreligger eller när cancerdiagnosen bekräftas skall patienten utredas med avseende på klinisk stadieindelning enligt FIGO (International Federation of Gynecology and Obstetrics) och planerad behandling. Undersökningar som får ligga till grund för stadieindelning enligt FIGO är (förutom klinisk undersökning) palpation i narkos, cystoskopi, urografi och lungröntgen. På särskild indikation kan även proktoskopi, rektoskopi och skelettröntgen göras. Numera görs även ultraljud, datortomografi och/eller magnetresonanstomografi av lilla bäckenet. Dessa undersökningar skall dock inte utnyttjas vid den kliniska stadieindelningen, men väl till val av behandling. Om CT görs kan den ersätta urografin för att fastställa eventuell urinvägspåverkan genom att kontrasten utsöndras via njurarna och därmed avslöjar eventuell stas. MR är bättre än CT för kartläggning av lokal tumörutbredning men är likvärdig vid lymfkörtelmetastasering. MR rekommenderas som utredning vid nydiagnostiserad cancer och kan även utnyttjas för att skilja tumörvävnad från fibros. Position emissionstomografi (PET) är ytterligare ett alternativ och förefaller vara överlägset både CT och MR vid utredning av förstorade lymfkörtlar.
På sjukhuskliniken görs en gynekologisk undersökning när patienten är sövd eller har ryggbedövning. Undersökningen görs oftast av ett team av läkare med särskild expertis på gynekologiska cancersjukdomar. Vid palpation i narkos görs bimanuell palpation, abrasio samt finnålspunktion av eventuella suspekta förändringar. Läkarteamet väger sedan samman fynden med röntgenbilder.
Stadium 0: Cancer in situ, intraepitelialt carcinom
Stadium I: Cancer enbart i cervix uteri (inklusive eventuellt corpusengagemang)
Stadium IA: Mikroskopisk invasion (djup max 5 mm och bredd max 7 mm)
Stadium IA1: Djup max 3 mm och bredd max 7 mm
Stadium IA2: Djup mer än 3 mm och max 5 mm samt bredd max 7 mm
Stadium IB: Tumörutbredning i cervix, större än IA
Stadium IB1: Tumör max 4 cm i storlek
Stadium IB2: Tumör större än 4 cm i storlek
Stadium II: Tumörengagemang av vaginas övre två tredjedelar eller parametrium, dock ej ut till bäckenväggen
Stadium IIA: Tumörengagemang av vagina, men ej parametrium
Stadium IIB: Tumörengagemang av parametrium
Stadium III: Tumörengagemang av vaginas nedre tredjedel, växt ut mot bäckenväggen eller hydronefros alternativt icke fungerande njure till följd av tumörväxt
Stadium IIIA: Tumörväxt i vaginas nedre tredjedel
Stadium IIIB: Tumörväxt ut mot bäckenväggen och/eller hydronefros alternativt njurpåverkan
Stadium IV: Tumörväxt utanför lilla bäckenet eller med engagemang av blås- alternativt rektalslemhinna
Stadium IVA: Tumörengagemang av blås- alternativt rektalslemhinna
Stadium IVB: Distansmetastaser eller växt utanför lilla bäckenet
Differentialdiagnoser till cervixcancer
Man kan ha småblödningar från underlivet av andra orsaker än livmoderhalscancer. De kan till exempel bero på användande av p-piller, hormonspiral eller att man har sköra slemhinnor, infektiösa eller inflammatoriska tillstånd eller, och kanske allra viktigast, corpuscancer.
Behandling
Traditionellt är standardbehandlingen av tidig cervixcancer (stadium I och II) intrakavitär och extern strålbehandling, primär kirurgi eller en kombination av strålbehandling och kirurgi. Vid kirurgi förekommer enkel hysterektomi eller olika grader av utvidgad hysterektomi med utrymning av lymfkörtlar i lilla bäckenet. Någon säker skillnad i resultat för stadium I eller II finns inte mellan strålbehandling och kirurgi eller kombinationer därav. Däremot rapporteras det en högre grad av morbiditet i de fall som erhållit både strålbehandling och kirurgi. Titthålsteknik, laparaskopi, blir allt vanligare och på allt fler kliniker kan operation göras med robotteknologi.
Cytostatika ges vid recidiv i tidigare strålbehandlat område vid disseminerad sjukdom i palliativt syfte. Försök med adjuvant kemoterapi har inte visat förbättrat resultat med bättre överlevnad, men däremot kan neoadjuvant kemoterapi ge god tumörreduktion och därmed underlätta eller möjliggöra kirurgisk intervention.
Vid avancerade stadier föredras primär strålbehandling. För lokal tumörkontroll krävs höga stråldoser med relativt stora risker för komplikationer. En skillnad i inställning finns avseende adenocarcinom och skivepitelcancer vid CIN III och tidig invasivitet. För adenocarcinom rekommenderas kallknivskonisering vid dysplasier och hysterektomi vid tidig eller misstänkt invasivitet (stadium IA1). Vid bristande radikalitet skall patienten reopereras med ny konisering alternativt hysterektomi.
Högdoserat brachyterapi (”inre” strålbehandling) ges med efterladdningsteknik med en stegande 192Ir-strålkälla. Vid applikation är patienten sövd eller i spinalanestesi. Targetvolymen (behandlingsområdet) definieras från tillgänglig diagnostisk information och palpation vid applikationstillfället.
Om man får extern (”yttre”) strålbehandling ges även cytostatika vanligtvis en gång i veckan. Det görs för att öka cancertumörens känslighet för strålning. Andra tillfällen då man kan få cytostatika är före operation, så kallad neoadjuvant behandling, för att krympa tumören, eller om sjukdomen kommer tillbaka efter behandling.
Prognosen vid återfall av cervixcancer är dålig och överlevnaden begränsad. Penetrationen av cytostatika inom tidigare strålbehandlat område är dålig och därför mindre verksamt vid lokalt recidiv. Recidivet ses i 40 procent utanför bäckenet. Behandling ges då med kemoterapi, eventuellt kombinerat med strålbehandling vid exempelvis skelett- eller lymfkörtelmetastaser. Patienter med recidiv och som tidigare fått kemoradioterapi uppvisar sämre behandlingsresultat, förmodligen på grund av resistensutveckling vid återbehandling med singeldrog cisplatin. Med denna utgångspunkt har studier med kombinationsbehandling genomförts.
GOG 179 visade att kombinationsbehandling med topotecan och cisplatin gav en signifikant bättre överlevnad; 9,4 månader jämfört med 6,5 månader vid singelbehandling med cisplatin. För patienter med gott allmäntillstånd är detta nu standardbehandling. Även annan kombination, såsom cisplatin och paklitaxel, har visats ge god respons men utan påvisad överlevnadsvinst.
Palliativ strålbehandling ges framför allt vid recidiv inom tidigare ej strålbehandlat område eller om behandling i området inte givits upp till fulldos. Framför allt gäller detta lymfkörtlar på halsen, fossa supraklavikulärt, paraaortalt eller i ljumskarna, där man kan uppnå god tumörregress och symtomlindring. Kotmetastaser och andra skelettmetastaser kan strålbehandlas i smärtlindrande syfte, med en engångsdos på 8 Gy alternativt en fraktionerad dos. Vid vaginal blödning kan man oftast ge en engångsdos i symtomlindrande syfte.
Prognos
Efter en behandling för livmoderhalscancer i botande syfte erbjuds kontroller regelbundet under fem år. De två första åren erbjuds vanligen återbesök var tredje till fjärde månad och därefter två gånger per år. Kontrollerna görs för att i tid upptäcka om cancern kommit tillbaka och för att upptäcka eventuella komplikationer som man kan ha fått av cancerbehandlingen.
Risken för recidiv är störst under de första tre åren efter avslutad behandling. I Sverige är den relativa femårsöverlevnaden cirka 70 procent och tioårsöverlevnaden cirka 65 procent.
Komplikationer
Alla operationer och cancerbehandlingar kan ge biverkningar. Dessa brukar delas in i tidiga (eller akuta) och sena (eller fördröjda). Efter operationen kan det blöda från slidan under två till tre veckor, liksom det finns risk för postoperativa infektioner. Under den tiden ska man inte använda tampong och man ska duscha istället för att bada. Man ska inte ha samlag på fyra till sex veckor.
Som vid alla operationer finns det även risk för att få infektioner i såret och blödningar, vilket kan gör att det tar extra lång tid att återhämta sig efter operationen. Allvarliga kirurgiska komplikationer är ovanliga. Den avancerade dissektionen vid radikal hysterektomi medför risker för såväl peroperativa som postoperativa komplikationer. I samband med ingreppet förekommer blödningar diffust eller till följd av skador på de stora kärlen. Skador på blåsa och uretärer förekommer också. Postoperativa komplikationer är infektion, miktionsstörningar, fistlar till blåsa eller uretärer, lymfocele, lymfödem och trombos.
Om äggstockarna tas bort induceras menopaus om inte patienten redan passerat klimakteriet. Då kan man få besvär med blodvallningar, svettningar och torra slemhinnor.
Besvär under och strax efter strålbehandling är vanligt. Man kan få sveda när man kissar, känna illamående, få diarré och bli trött.
Med sena biverkningar avses de som uppkommer eller kvarstår månader efter avslutad strålbehandling. Besvären kan ibland debutera flera år efter avslutad behandling. Vanligast är strålinducerade förändringar på tarmen. Den akuta strålreaktionen beror på utarmning av stamceller i tarmkryptorna, medan den sena reaktionen orsakas av kärlförändringar som leder till atrofi av mukosan och fibros i muskellagret. Tunntarmsslyngor som är fixerade av postoperativa sammanväxningar är mer känsliga för strålning.
Lymfödem i benen är ett svårbehandlat men vanligt tillstånd vid cervixcancer. Detta kan uppkomma efter lymfkörtelutrymning eller strålbehandling mot lymfkörtelstationerna eller på grund av tumörspridning till regionala lymfknutor. Tidiga tecken på lymfödem är inte alltid svullnad, utan kan vara symtom såsom ökad trötthets-, tyngd- eller spänningskänsla i benet.
Fistelbildningar förekommer, men numera oftare vid recidiv än som behandlingskomplikation. Vesikovaginala fistlar är vanligast.
Studier har visat en något ökad risk hos långtidsöverlevande (>10 år) att utveckla sekundär malignitet i urinblåsa, endometrium, ovarier och rektum, men inte colon.
Av cytostatika som ges vid livmoderhalscancer tappar man sällan håret, men vanligt är illamående, infektionskänslighet och trötthet.
Särskilda och/eller förebyggande råd
Genom att lämna cellprov kan cellförändringar upptäckas och behandlas innan cancer har utvecklats. Det finns idag två vacciner i Sverige som skyddar mot HPV-typerna 16 och 18. Det ena vaccinet, Gardasil, ger även skydd mot kondylom, medan det andra, Cervarix, också ger ett visst skydd mot några andra HPV-typer som kan orsaka cancer i livmoderhalsen.
Vaccination kan också ge ett visst skydd mot bland annat analcancer, peniscancer och tonsillcancer. För att vaccinet ska ge ett skydd, ska man inte vara smittad med HPV. Därför är det bäst att vaccinera sig innan man har haft sex första gången. Man kan vaccinera sig även om man har haft sex - men ju fler sexuella kontakter man haft, desto mindre nytta har man av vaccinationen.
Eftersom vaccinationen inte ger ett fullständigt skydd mot livmoderhalscancer, är det viktigt att gå på de cellprovskontroller som man blir kallad till.
ICD-10
Malign tumör i livmoderhalsen (C53)
C53.0: Malign tumör i endocervix
C53.1: Malign tumör i exocervix
C53.8: Malign tumör i cervix uteri med övergripande växt
C53.9: Icke specificerad lokalisation av malign tumör i cervix uteri
Cancer in situ i livmoderhalsen (D06)
D06.0: Cancer in situ i endocervix
D06.1: Cancer in situ i exocervix
D06.7: Cancer in situ i andra delar av cervix
D06.9: Icke specificerad lokalisation av cancer in situ i cervix
Dysplasi i cervix uteri (livmoderhalsen) (N87)
N87.0: Lätt dysplasi i cervix
N87.1: Måttlig dysplasi i cervix
N87.2: Svår dysplasi i cervix som ej klassificeras annorstädes
N87.9: Dysplasi i cervix uteri, ospecificerad
Referenser
Cancer incidence in Sweden 2013, Socialstyrelsen
Cancer incidence in Sweden 2000, Socialstyrelsen
Dödsorsaker 2012, Socialstyrelsen
Richart RM, Am J Obstet Gynecol 1969, 105(3):386-393
VP norr cervixcancer (2012)
Cervix_vulva_vagina_ Skåne (2010)
Björn Strander, Läkartidningen nr 10 2011 volym 108 pp 533-535



